


Vial de la vacuna contra la COVID-19 de Pfizer-BioNTech per al mercat nord-americĂ
|
|
| DescripciĂł de la vacuna | |
|---|---|
| Blanc | SARS-CoV-2 |
| Tipus de vacuna | ARNm |
| Dades clĂniques | |
| Noms comercials | Comirnaty[1][2][3] |
| Altres noms | BNT162b2, vacuna d'ARNm COVID-19 (modificada amb nucleĂČsid), vacuna COVID-19 (ARNm)[4] |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | A621003 |
| Dades de la llicĂšncia | |
Categoria d'embarĂ s |
|
| Vies d'administraciĂł |
Intramuscular |
| Codi ATC | |
| RĂšgim jurĂdic | |
| RĂšgim jurĂdic |
|
| Identificadors | |
| NĂșmero CAS | |
| SID de PubChem | |
| Banc de drogues | |
| UNII | |
| KEGG | |
| ChEMBL | |
La vacuna contra la COVID-19 de Pfizer-BioNTech, venuda sota la marca Comirnaty,[2][29] Ă©s una vacuna COVID-19 basada en ARNm desenvolupada per l'empresa biotecnolĂČgica alemanya BioNTech. Per al seu desenvolupament, BioNTech va col·laborar amb l'empresa nord-americana Pfizer per dur a terme assajos clĂnics, logĂstica i fabricaciĂł. [41][42] EstĂ autoritzat per al seu Ășs en persones per proporcionar protecciĂł contra la COVID-19, causada per la infecciĂł amb el virus SARS-CoV-2. [2][27] La vacuna s'administra per injecciĂł intramuscular. [31] Es compon d'ARNm modificat per nucleĂČsids (modRNA) que codifiquen una forma mutada de la proteĂŻna espiga de longitud completa del SARS-CoV-2, que estĂ encapsulada en nanopartĂcules lipĂdiques. [43] El consell inicial indicava que la vacunaciĂł requeria dues dosis administrades amb 21 dies de diferĂšncia,[31][44][45][46] perĂČ l'interval es va ampliar mĂ©s tard fins a 42 dies als EUA,[31][47] i fins a quatre mesos al CanadĂ . [48][49]
Els assajos clĂnics van començar a l'abril de 2020; [44] Al novembre de 2020, la vacuna va entrar en assajos clĂnics de fase III, amb mĂ©s de 40.000 persones participants. [50] Una anĂ lisi provisional de les dades de l'estudi va mostrar una eficĂ cia potencial del 91.3% en la prevenciĂł de la infecciĂł simptomĂ tica dins dels set dies posteriors a una segona dosi i sense problemes greus de seguretat. [46][51] La majoria dels efectes secundaris sĂłn lleus a moderats en gravetat i desapareixen en pocs dies. [2][52] Els mĂ©s comuns inclouen dolor lleu a moderat en el lloc de la injecciĂł, fatiga i mals de cap. [53][54] Els informes d'efectes secundaris greus, com ara reaccions al·lĂšrgiques, sĂłn molt rars[a] i no s'han reportat complicacions a llarg termini. [2][56]
La vacuna Ă©s la primera vacuna contra la COVID-19 autoritzada per una autoritat reguladora estricta per a Ășs d'emergĂšncia[57][58] i la primera autoritzada per a un Ășs regular. [38] El desembre de 2020, el Regne Unit va ser el primer paĂs a autoritzar-ne l'Ășs de manera d'emergĂšncia. [56] EstĂ autoritzat per al seu Ășs en algun nivell en la majoria de paĂŻsos. [59][60][61][62] El 23 d'agost de 2021, la vacuna de Pfizer-BioNTech es va convertir en la primera vacuna contra la COVID-19 aprovada als Estats Units per l'AdministraciĂł d'Aliments i Medicaments (FDA). [26][29][63] La distribuciĂł i emmagatzematge Ă©s un repte logĂstic perquĂš la vacuna necessita emmagatzemar-se a temperatures extremadament baixes. [64]
L'agost del 2022 es va autoritzar una versiĂł bivalent de la vacuna (Pfizer-BioNTech COVID-19 Vaccine, Bivalent) per al seu Ășs com a dosi de reforç en persones de dotze anys o mĂ©s als Estats Units. [65][66][67][68] El setembre de 2022, la versiĂł BA.1 de la vacuna bivalent (Comirnaty Original/Omicron BA.1 o tozinameran/riltozinameran)[69] va ser autoritzada com a reforç per al seu Ășs al Regne Unit. [70][71][72] El setembre de 2022, la UniĂł Europea va autoritzar tant les versions de reforç BA.1 com BA.4/BA.5 (tozinameran/famtozinameran) de la vacuna bivalent. [2][3][37]
La vacuna contra la COVID-19 de Pfizer-BioNTech s'utilitza per proporcionar protecció contra la COVID-19, causada per la infecció pel virus SARS-CoV-2, provocant una resposta immunità ria a l'antigen S. [1][2][27][36] La vacuna s'utilitza per reduir la morbimortalitat per COVID-19. [31]
La vacuna es subministra en un vial multidosi com "una suspensió blanca a blanca, estÚril, sense conservants, congelada per a la injecció intramuscular". [27][36][73] S'ha de descongelar a temperatura ambient i diluir-lo amb sÚrum salà normal abans de l'administració. [36][73]
El curs inicial consta de dues dosis. [31][36] L'OrganitzaciĂł Mundial de la Salut (OMS) recomana un interval de tres a quatre setmanes entre dosis. Retardar fins a dotze setmanes la segona dosi augmenta la immunogenicitat, fins i tot en adults grans, contra totes les variants preocupants. [74] Els autors de l'estudi Pitch pensen que l'interval ĂČptim contra la variant Delta Ă©s d'unes vuit setmanes, amb intervals mĂ©s llargs que deixen els receptors vulnerables entre dosis. [74]
Es pot afegir una tercera, quarta o cinquena dosi en alguns paĂŻsos. [65][75][76][77][78][79]
|
|
Aquesta secció necessita referÚncies mÚdiques addicionals per a la seva verificació. (Novembre 2021)
|
Un estudi de casos i controls negatiu[nota 1] publicat l'agost del 2021 va trobar que dues dosis de la vacuna BNT162b2 (Pfizer) tenien una efectivitat del 93,7% contra la malaltia simptomà tica causada per la variant alfa (B.1.1.7) i del 88,0% contra la malaltia simptomà tica causada per la variant delta (B.1.617.2). [80] Cal destacar que l'efectivitat després d'una dosi de la vacuna de Pfizer va ser del 48,7% contra l'alfa i del 30,7% contra la delta, similar a l'efectivitat proporcionada per una dosi de la vacuna ChAdOx1 nCoV-19. [81]
El 27 d'agost, els Centres per al Control i la Prevenció de Malalties dels Estats Units (CDC) van publicar un estudi que informava que l'efectivitat contra la infecció va disminuir del 91% (81-96%) al 66% (26-84%) quan la variant Delta es va convertir en predominant als EUA, cosa que pot ser deguda a una confusió residual i no mesurada relacionat amb una disminució de l'efectivitat de la vacuna al llarg del temps. [82]
Llevat que s'indiqui el contrari, les segĂŒents qualificacions d'efectivitat sĂłn indicatives d'eficĂ cia clĂnica dues setmanes desprĂ©s de la segona dosi. Una vacuna es considera generalment eficaç si l'estimaciĂł Ă©s del â„50% amb un lĂmit >30% inferior de l'interval de confiança del 95%. [83] En general, s'espera que l'eficĂ cia disminueixi lentament amb el temps. [84]
| Dosis | Gravetat de la malaltia | Alfa | Beta | Gamma | Delta | Ămicron | Altres que circulaven anteriorment[A] |
|---|---|---|---|---|---|---|---|
| 1 | AsimptomĂ tic | 38% (29â45%)[86] | 17% (10â23%)[87] | No denunciat | 30% (17â41%)[86] | No denunciat | 60% (53â66%) |
| SimptomĂ tic | 27% (13â39%)[86] | 43% (22â59%)[88] | 33% (15â47%)[86] | No denunciat | 66% (57â73%) | ||
| HospitalitzaciĂł | 83% (62â93%)[B] | 0% (0â19%)[87] | 56% (â9 a 82%)[88] | 94% (46â99%)[B] | No denunciat | 78% (61â91%) | |
| 2 | AsimptomĂ tic | 92% (90â93%)[86] | 75% (71â79%)[87] | No denunciat | 79% (75â82%)[86] | No denunciat | 92% (88â95%) |
| SimptomĂ tic | 92% (88â94%)[86] | 88% (61â96%)[88] | 83% (78â87%)[86] | 88% (66â96%)[C] | 94% (87â98%) | ||
| HospitalitzaciĂł | 95% (78â99%)[B] | 100% (74â100%)[87] | 100%[D][88] | 96% (86â99%)[B] | 70% (62â76%)[92] | 87% (55â100%) | |
| 3[E] | SimptomĂ tic | No denunciat | No denunciat | No denunciat | 96% (89â99%)[F] | 76% (56â86%)[G] | No denunciat |
El 12 de novembre, Public Health England va informar d'una possible perĂČ extremadament petita reducciĂł en l'eficĂ cia contra la malaltia simptomĂ tica del subllinatge Delta AY.4.2 a intervals mĂ©s llargs desprĂ©s de la segona dosi. [95]
Les dades preliminars suggereixen que l'efectivitat contra la variant ĂČmicron comença a disminuir en unes 10 setmanes, ja sigui desprĂ©s de la pauta inicial de dues dosis o desprĂ©s de la dosi de reforç. [91][94] Per a altres variants, l'efectivitat de les dosis inicials comença a disminuir en uns sis mesos. [96] Un estudi de casos i controls a Qatar de l'1 de gener al 5 de setembre de 2021 va trobar que l'efectivitat contra la infecciĂł va assolir un mĂ xim del 78% (IC 95%, 76-79%) el primer mes desprĂ©s de la segona dosi, seguida d'un lent descens que es va accelerar desprĂ©s del quart mes, arribant al 20% als mesos 5 a 7. Es va observar una trajectĂČria similar contra la malaltia simptomĂ tica i contra variants especĂfiques. L'efectivitat contra la malaltia greu, l'hospitalitzaciĂł i la mort va ser mĂ©s robusta, arribant a un mĂ xim del 96% (93-98%) en el segon mes i mantenint-se gairebĂ© estable fins al sisĂš mes, disminuint a partir de llavors. [97]
El 21 d'octubre, un assaig de fase 3 va mostrar que una dosi de reforç administrada aproximadament 11 mesos després de la segona dosi va restaurar l'efecte protector al nivell d'eficà cia del 96% (IC 95%, 89-99%) contra la malaltia simptomà tica de la variant Delta. [98][93]
El 8 de desembre, Pfizer i BioNTech van informar que les dades preliminars indicaven que una tercera dosi de la vacuna proporcionaria un nivell similar d'anticossos neutralitzants contra la variant ĂČmicron vist desprĂ©s de dues dosis contra altres variants. [99]
El 14 de desembre, l'asseguradora de salut privada Discovery Health, en col·laboraciĂł amb el Consell de Recerca MĂšdica de Sud-Ă frica, va informar que les dades del mĂłn real de mĂ©s de 211.000 casos de COVID-19 a Sud-Ă frica, dels quals 78.000 eren de la variant ĂČmicron, indiquen que l'efectivitat contra la variant desprĂ©s de dues dosis Ă©s del voltant del 70% contra l'ingrĂ©s hospitalari i del 33% contra la malaltia simptomĂ tica. Es mantĂ© la protecciĂł contra l'ingrĂ©s hospitalari per a totes les edats i col·lectius amb comorbiditats. [100]
A study of the bivalent booster effectiveness against severe COVID-19 outcomes in Finland, September 2022âJanuary 2023, has shown that it reduced the risk of severe COVID-19 outcomes among the elderly. By contrast, among the chronically-ill 18â64-year-olds the risk was similar among those who received bivalent vaccine and those who did not. Among the elderly a bivalent booster provided highest protection during the first two months after vaccination, but thereafter signs of waning were observed. The effectiveness among individuals aged 65â79 years and those aged 80 years or more was similar.[101]
Based on the results of a preliminary study, the U.S. Centers for Disease Control and Prevention (CDC) recommends that pregnant women get vaccinated with the COVIDâ19 vaccine.[102][103]
A statement by the British Medicines and Healthcare products Regulatory Agency (MHRA) and the Commission on Human Medicines (CHM) reported that the two agencies had reached a conclusion that the vaccine is safe and effective in children aged between 12 and 15 years.[104][105]
On 19 May 2021, experts commissioned by the Norwegian Medicines Agency concluded that the Pfizer-BioNTech vaccine is the likely cause of ten deaths of frail elderly patients in Norwegian nursing homes. They said that people with very short life expectancies have little to gain from vaccination, having a real risk of adverse reactions in the last days of life and of dying earlier.[106]
A 2021 report by the New South Wales Government (NSW Health) in Australia found that the Pfizer-BioNTech vaccine is safe for those with various forms of immunodeficiency or immunosuppression, though it does note that the data on said groups is limited, due to their exclusion from many of the vaccine earlier trials held in 2020. It notes that the World Health Organization advises that the vaccine is among the three COVID-19 vaccines (alongside that of Moderna and AstraZeneca) it deems safe to give to immunocompromised individuals, and that expert consensus generally recommends their vaccination. The report states that the vaccines were able to generate an immune response in those individuals, though it does also note that this response is weaker than in those that are not immunocompromised. It recommends that specific patient groups, such as those with cancer, inflammatory bowel disease and various liver diseases be prioritised in the vaccination schedules over other patients that do not have said conditions.[107]
On 20 September 2021, Pfizer announced that a clinical trial conducted in more than 2,200 children aged 5â11 has generated a "robust" response and is safe.[108][109]
En els assajos de fase 3 de la vacuna no es van reportar troballes greus de seguretat i es va observar una baixa incidĂšncia d'esdeveniments adversos greus. [46][51]
La majoria dels efectes secundaris de la vacuna contra la COVID-19 de Pfizer-BioNTech sĂłn de gravetat lleu a moderada i desapareixen en pocs dies. [52][2] SĂłn similars a altres vacunes per a adults i sĂłn signes normals que el cos estĂ construint protecciĂł contra el virus. [52] Durant els assaigs clĂnics, els efectes secundaris comuns que afecten mĂ©s d'1 de cada 10 persones sĂłn (per ordre de freqĂŒĂšncia): dolor i inflor al lloc de la injecciĂł, cansament, mal de cap, dolors musculars, calfreds, dolor articular i febre. [110] La febre Ă©s mĂ©s freqĂŒent desprĂ©s de la segona dosi. [110]
L'AgĂšncia Europea del Medicament (EMA) revisa periĂČdicament les dades sobre la seguretat de la vacuna. L'informe de seguretat publicat el 8 de setembre de 2021 per l'EMA es va basar en mĂ©s de 392 milions de dosis administrades a la UniĂł Europea. [2] Segons l'EMA, "els beneficis de Comirnaty en la prevenciĂł de la COVID-19 continuen superant qualsevol risc, i no hi ha canvis recomanats pel que fa a l'Ășs d'aquesta vacuna". [2] Els efectes secundaris rars (que poden afectar fins a 1 de cada 1.000 persones) inclouen caiguda facial temporal d'una sola cara i reaccions al·lĂšrgiques com urticĂ ria o inflor de la cara. [2]
La hipersensibilitat documentada al polietilenglicol (PEG) (una al·lÚrgia molt rara) figura com a contraindicació a la vacuna de Pfizer COVID-19. [111] S'ha observat una reacció al·lÚrgica greu en aproximadament onze casos per milió de dosis de vacuna administrades. [112][113] Segons un informe dels Centres per al Control i la Prevenció de Malalties dels Estats Units, el 71% d'aquestes reaccions al·lÚrgiques es van produir als 15 minuts de la vacunació i majorità riament (81%) entre persones amb antecedents documentats d'al·lÚrgies o reaccions al·lÚrgiques. [112] L'AgÚncia Reguladora de Medicaments i Productes Sanitaris del Regne Unit (MHRA) va aconsellar el 9 de desembre de 2020 que les persones que tinguin antecedents de reacció al·lÚrgica "significativa" no haurien de rebre la vacuna contra la COVID-19 de Pfizer-BioNTech. [114][115][116] El 12 de desembre, el regulador canadenc va fer el mateix, assenyalant que: "Tots dos individus al Regne Unit tenien antecedents de reaccions al·lÚrgiques greus i portaven injectors automà tics d'adrenalina. Tots dos van ser atesos i s'han recuperat". [117]
El juny del 2021, el Ministeri de Salut d'Israel va anunciar una probable relació entre la segona dosi i la miocarditis en un petit grup d'homes de 16 a 30 anys. [118] Entre desembre de 2020 i maig de 2021, hi va haver 55 casos de miocarditis per cada 1 milió de persones vacunades, el 95% de les quals es van classificar com a lleus i la majoria no van passar més de quatre dies a l'hospital. [118] Des d'abril de 2021, s'han notificat un nombre creixent de casos de miocarditis i pericarditis als Estats Units en aproximadament un 1,8 % de vacunats, majorità riament homes i majors de 16 anys, després de la vacunació amb la vacuna de Pfizer-BioNTech o la vacuna de Moderna. [119][120] La majoria de les persones afectades es recuperen rà pidament amb un tractament i descans adequats.[121]
La tecnologia BioNTech per a la vacuna BNT162b2 es basa en l'Ășs d'ARNm modificat per nucleĂČsids (modRNA) que codifica una forma mutada de la proteĂŻna espiga de longitud completa que es troba a la superfĂcie del virus SARS-CoV-2,[123] desencadenant una resposta immunitĂ ria contra la infecciĂł per la proteĂŻna del virus. [124]
La seqĂŒĂšncia de modRNA de la vacuna tĂ© una longitud de 4.284 nucleĂČtids. [125] Consisteix en un casquet de cinc primers; una regiĂł no traduĂŻda de cinc primers derivada de la seqĂŒĂšncia de globina alfa humana; un pĂšptid senyal (bases 55-102) i dues substitucions de prolina (K986P i V987P, designades "2P") que fan que l'espiga adopti una conformaciĂł estabilitzada per prefusiĂł reduint la capacitat de fusiĂł de membrana, augmentant l'expressiĂł i estimulant anticossos neutralitzants; [43][126] un gen optimitzat per codĂł de la proteĂŻna espiga de longitud completa del SARS-CoV-2 (bases 103â3879); seguit d'una regiĂł no traduĂŻda de tres primers (bases 3880â4174) combinades d'AES i mtRNR1 seleccionades per augmentar l'expressiĂł de proteĂŻnes i l'estabilitat de l'ARNm[127] i una cua poli(A) que comprĂšn 30 residus d'adenosina, una seqĂŒĂšncia enllaçadora de 10 nucleĂČtids i altres 70 residus d'adenosina (bases 4175â4284). [125] La seqĂŒĂšncia no contĂ© residus d'uridina; SĂłn substituĂŻts per 1-metil-3'-pseudouridilil. [125] Les substitucions de prolina 2P a les proteĂŻnes espiga van ser desenvolupades originalment per a una vacuna de la sĂndrome respiratĂČria de l'Orient MitjĂ (MERS) per investigadors del Centre d'InvestigaciĂł de Vacunes de l'Institut Nacional d'Al·lĂšrgies i Malalties Infeccioses, Scripps Research i l'equip de Jason McLellan (a la Universitat de Texas a Austin, anteriorment al Dartmouth College). [126]
A mĂ©s de la molĂšcula d'ARNm, la vacuna contĂ© els segĂŒents ingredients inactius (excipients):[23][117][110]
Els quatre primers sĂłn lĂpids. Els lĂpids i el modRNA junts formen nanopartĂcules que actuen no nomĂ©s com a portadors per fer arribar el modRNA a les cĂšl·lules humanes, sinĂł tambĂ© com a adjuvants. [128] ALC-0159 Ă©s un conjugat de polietilenglicol, Ă©s a dir, un lĂpid PEGilat. [129]
 Un soldat nord-americĂ sostenint la vacuna de Pfizer-BioNTech
Un soldat nord-americĂ sostenint la vacuna de Pfizer-BioNTech
Pfizer i BioNTech estan fabricant la vacuna a les seves prĂČpies instal·lacions als Estats Units i a Europa. La llicĂšncia per distribuir i fabricar la vacuna a la Xina va ser comprada per Fosun, juntament amb la seva inversiĂł en BioNTech. [42][130]
La fabricaciĂł de la vacuna requereix un procĂ©s de tres etapes. La primera etapa consisteix en la clonaciĂł molecular de plasmidis d'ADN que codifiquen per a la proteĂŻna espiga infonent-los en bacteris Escherichia coli. Per a tots els mercats, aquesta etapa es porta a terme als Estats Units,[131] en una petita planta pilot de Pfizer a Chesterfield, Missouri[132][133] (prop de St. Louis). DesprĂ©s de quatre dies de creixement, els bacteris es maten i s'obren, i el contingut de les seves cĂšl·lules es purifica durant una setmana i mitja per recuperar el producte d'ADN desitjat. L'ADN s'embotella i es congela per al seu enviament. El transport segur i rĂ pid de l'ADN en aquesta etapa Ă©s tan important que Pfizer ha utilitzat el seu aviĂł i helicĂČpter de la seva companyia per ajudar-lo. [134]
La segona etapa s'estĂ duent a terme en una planta de Pfizer a Andover, Massachusetts,[135] als Estats Units, i a les plantes de BioNTech a Alemanya. [131] L'ADN s'utilitza com a plantilla per construir les cadenes d'ARNm desitjades,[134] que triga uns quatre dies. [131] Un cop creat i purificat l'ARNm, es congela en bosses de plĂ stic aproximadament de la mida d'una bossa de la compra gran, de les quals cadascuna pot contenir fins a 10 milions de dosis. Les bosses es col·loquen en camions que les porten a la segĂŒent planta. [134]
 Un empleat de Pfizer posant gel sec en una caixa per protegir les vacunes contra la COVID-19 durant el transport a la fĂ brica de Puurs
Un empleat de Pfizer posant gel sec en una caixa per protegir les vacunes contra la COVID-19 durant el transport a la fĂ brica de Puurs Caixes amb les vacunes contra la COVID-19 a la fĂ brica de Pfizer a Puurs
Caixes amb les vacunes contra la COVID-19 a la fĂ brica de Pfizer a Puurs Vista interior de la fĂ brica Pfizer a Puurs
Vista interior de la fĂ brica Pfizer a Puurs
La tercera etapa s'estĂ duent a terme a les plantes de Pfizer a Portage, Michigan[136] (prop de Kalamazoo) als Estats Units, i Puurs a BĂšlgica. Aquesta etapa consisteix a combinar l'ARNm amb nanopartĂcules lipĂdiques, desprĂ©s omplir vials, vials de boxa i congelar-los. [134] La filial de Croda International, Avanti Polar Lipids, proporciona els lĂpids necessaris. [137] A partir de novembre de 2020, el principal coll d'ampolla en el procĂ©s de fabricaciĂł Ă©s combinar ARNm amb nanopartĂcules lipĂdiques. [134] En aquesta etapa, nomĂ©s es necessiten quatre dies per passar de l'ARNm i els lĂpids als vials acabats, perĂČ cada lot ha de passar diverses setmanes en emmagatzematge ultracongelat mentre se sotmet a una verificaciĂł contra 40 mesures de control de qualitat. [131]
Abans de maig de 2021,[138] la planta de Pfizer a Puurs era responsable de tots els vials de destinacions fora dels Estats Units. [131] Per tant, totes les dosis administrades a AmÚrica fora dels Estats Units abans d'aquest moment requerien almenys dos vols transatlà ntics (un per portar ADN a Europa i un altre per portar vials de vacuna acabats). [131]
El febrer de 2021, BioNTech va anunciar que augmentaria la producció en més d'un 50% per fabricar 2.000 milions de dosis el 2021,[139] augmentades de nou a finals de març fins als 2.500 milions de dosis el 2021. [140]
El febrer del 2021, Pfizer va revelar que tota la seqĂŒĂšncia va trigar inicialment uns 110 dies de mitjana de principi a fi i que la companyia avança en la reducciĂł del temps a 60 dies. [141] MĂ©s de la meitat dels dies del procĂ©s de producciĂł es dediquen a proves rigoroses i garantia de qualitat en cadascuna de les tres etapes. [141] Pfizer tambĂ© va revelar que el procĂ©s requereix 280 components i es basa en 25 proveĂŻdors ubicats a 19 paĂŻsos. [131]
Els fabricants de vacunes normalment triguen diversos anys a optimitzar el procés de fabricació d'una vacuna particular per obtenir velocitat i cost-efectivitat abans d'intentar la producció a gran escala. [141] A causa de la urgÚncia presentada per la pandÚmia COVID-19, Pfizer i BioNTech van començar la producció immediatament amb el procés pel qual la vacuna s'havia formulat originalment al laboratori, i després van començar a identificar maneres d'accelerar i ampliar aquest procés de manera segura. [141]
 Xeringues que contenen dosis de la vacuna contra la COVID-19 de Pfizer
Xeringues que contenen dosis de la vacuna contra la COVID-19 de Pfizer
BioNTech va anunciar el setembre de 2020 que havia signat un acord per adquirir una planta de fabricació a Marburg, Alemanya, de Novartis per ampliar la seva capacitat de producció de vacunes. [142] Un cop completament operativa, la instal·lació produiria fins a 750 milions de dosis a l'any, o més de 60 milions de dosis al mes. El lloc serà la tercera instal·lació de BioNTech a Europa que produeix la vacuna, mentre que Pfizer opera almenys quatre centres de producció als Estats Units i Europa. [142]
La instal·laciĂł de Marburg s'havia especialitzat prĂšviament en immunoterĂ pia contra el cĂ ncer per a Novartis. [143] A finals de març de 2021, BioNTech havia acabat d'adaptar la instal·laciĂł per a la producciĂł de vacunes d'ARNm i reciclar els seus 300 empleats, i va obtenir l'aprovaciĂł per començar a fabricar. [143] A mĂ©s de fabricar ARNm, la instal·laciĂł de Marburg tambĂ© realitza el pas de combinar ARNm amb lĂpids per formar nanopartĂcules lipĂdiques, i desprĂ©s envia la vacuna a granel a altres instal·lacions per omplir-la i acabar-la (Ă©s a dir, omplir i boxejar vials). [143]
El 23 d'abril de 2021, l'EMA va autoritzar un augment de la mida del lot i l'ampliació del procés associat a la planta de Pfizer a Puurs. S'espera que aquest augment tingui un impacte significatiu en el subministrament de la vacuna a la Unió Europea. [144][145]
A finals d'abril del 2021, es va informar que Pfizer havia començat a exportar dosis de vacunes a MÚxic i Canadà des de la planta de Kalamazoo, molt més propera geogrà ficament als dos països que la planta de Puurs. [138]
La vacuna s'administra en vials que, una vegada diluĂŻts, contenen 2,25 ml de vacuna, compostos per 0,45 ml congelats i 1,8 ml de diluent. [146] Segons les etiquetes dels vials, cada vial contĂ© cinc dosis de 0,3 mL, perĂČ l'excĂ©s de vacuna es pot utilitzar per a una, o possiblement dues, dosis addicionals. [146][147] Ăs preferible l'Ășs de xeringues de baix espai mort per obtenir les dosis addicionals, i s'han de descartar dosis parcials dins d'un vial. [146][148] L'AgĂšncia Italiana del Medicament va autoritzar oficialment l'Ășs de dosis sobrants en vials Ășnics. [149] L'Autoritat SanitĂ ria Danesa permet barrejar dosis parcials de dos vials. [150] A 8 de gener de 2021, cada vial contĂ© sis dosis. [110][151][152][148] Als Estats Units, els vials es comptabilitzaran com a cinc dosis quan s'acompanyin de xeringues regulars i com a sis dosis quan s'acompanyin de xeringues d'espai mort baix. [153]
 La vacuna de Pfizer-BioNTech s'ha de mantenir a temperatures extremadament baixes per garantir l'eficà cia, aproximadament entre -80 i -60 °C (-112 i -76 °F).
La vacuna de Pfizer-BioNTech s'ha de mantenir a temperatures extremadament baixes per garantir l'eficà cia, aproximadament entre -80 i -60 °C (-112 i -76 °F).
La vacuna es pot emmagatzemar a 2 a 8 °C (36 a 46 °F) durant trenta dies abans de l'Ășs[154][155] i a 25 °C (77 °F)[23][27] o 30 °C (86 °F) [156][8] fins a dues hores abans de l'Ășs. Durant la distribuciĂł, la vacuna s'emmagatzema en contenidors especials que mantenen temperatures entre -80 i -60 °C (-112 i -76 °F). [157]
Els paĂŻsos de baixos ingressos tenen una capacitat limitada de la cadena de fred per al transport ultrafred i l'emmagatzematge d'una vacuna. [158] Les temperatures d'emmagatzematge necessĂ ries per a la vacuna[157][159][158][160][161] sĂłn molt mĂ©s baixes que per a la vacuna similar de Moderna. El cap de Bio Farma d'IndonĂšsia, Honesti Basyir, va dir que la compra de la vacuna estĂ fora de dubte per al quart paĂs mĂ©s poblat del mĂłn, ja que no tenia la capacitat necessĂ ria de la cadena de fred. De la mateixa manera, la xarxa de cadena de fred existent a l'Ăndia nomĂ©s pot gestionar temperatures entre 2 i 8 ° C (36 i 46 ° F), molt per sobre dels requisits de la vacuna. [162][163]
Abans de les vacunes contra la COVID-19, mai abans s'havia produĂŻt una vacuna per a una malaltia infecciosa en menys de diversos anys i no existia cap vacuna per prevenir una infecciĂł per coronavirus en humans. [164] El virus SARS-CoV-2, que causa la COVID-19, es va detectar el desembre de 2019,[165] i BioNTech va començar el desenvolupament d'una vacuna contra la COVID-19 el 10 de gener de 2020, quan el Centre XinĂšs per al Control i la PrevenciĂł de Malalties va publicar les seqĂŒĂšncies genĂštiques del SARS-CoV-2 provocant una resposta internacional urgent per preparar-se per a un brot i accelerar el desenvolupament de vacunes preventives. [166][167]
El desenvolupament de la vacuna va començar quan el fundador de BioNTech, UÄur Ćahin, va llegir un article a la revista mĂšdica The Lancet que el va convĂšncer que el coronavirus COVID-19 a la Xina aviat es convertiria en una pandĂšmia mundial, per la qual cosa va demanar als cientĂfics de la companyia que cancel·lessin les seves vacances i comencessin el desenvolupament d'una vacuna contra la COVID-19 el gener del 2020. [168] BioNTech va iniciar el seu programa 'Project Lightspeed' per desenvolupar una vacuna contra el nou virus COVID-19 basada en la seva tecnologia d'ARNm ja establerta,[50] que havien estat desenvolupant des que la investigadora lĂder d'ARNm Katalin KarikĂł es va unir a la companyia el 2013. [169] Es van crear diverses variants de la vacuna als seus laboratoris de MagĂșncia, i 20 d'elles es van presentar a experts de l'Institut Paul Ehrlich de Langen. [170]
Mentrestant, des del 2018, Pfizer havia estat treballant amb BioNTech en el desenvolupament d'una vacuna d'ARNm per a la grip, perĂČ els consellers delegats de les dues empreses no es van conĂšixer personalment fins que va arribar la COVID-19. [171] DesprĂ©s d'algunes trucades telefĂČniques, el conseller delegat de Pfizer, Albert Bourla, i Ćahin van acordar que les seves empreses treballarien juntes en el desenvolupament de la vacuna COVID-19 de BioNTech. [171] Els dos van acordar començar a treballar immediatament, sense cap acord legal formal per escrit per regir la nova col·laboraciĂł. [171] BioNTech va transferir el seu coneixement a Pfizer l'endemĂ . [171] Tres setmanes desprĂ©s es va signar una carta d'intencions i el gener de 2021 es va signar l'acord comercial formal entre Pfizer i BioNTech per a la vacuna contra la COVID-19. [171]
According to Pfizer, research and development for the vaccine cost close to US$1 billion.[172]
BioNTech received a US$135 million investment from Fosun in March 2020, in exchange for 1.58 million shares in BioNTech and the future development and marketing rights of BNT162b2 in China.[173][130]
In April 2020, BioNTech signed a partnership with Pfizer and received $185 million, including an equity investment of approximately $113 million.[174][175][176]
In June 2020, BioNTech received âŹ100 million (US$119 million) in financing from the European Commission and European Investment Bank.[177] The Bank's deal with BioNTech started early in the pandemic, when the Bank's staff reviewed its portfolio and came up with BioNTech as one of the companies capable of developing a COVIDâ19 vaccine. The European Investment Bank had already signed a first transaction with BioNTech in 2019.[178]
In September 2020, the German government granted BioNTech âŹ375 million (US$445 million) for its COVIDâ19 vaccine development program.[179]
El conseller delegat de Pfizer, Albert Bourla, va dir que va decidir no rebre fons de l'OperaciĂł Warp Speed del govern nord-americĂ per al desenvolupament de la vacuna "perquĂš volia alliberar els nostres cientĂfics [de] qualsevol burocrĂ cia que comporti haver de donar informes i acordar com gastarem els diners en paral·lel o junts, etc." Pfizer sĂ que va arribar a un acord amb els EUA per a l'eventual distribuciĂł de la vacuna, igual que amb altres paĂŻsos. [180]
Els assajos de fase I-II es van iniciar a Alemanya el 23 d'abril de 2020 i als Estats Units el 4 de maig de 2020, amb quatre candidats a vacuna que van entrar en proves clĂniques. [44][50] La candidata a vacuna BNT162b2 va ser escollida com la mĂ©s prometedora entre altres tres amb tecnologia similar desenvolupada per BioNTech. [124] Abans de triar BNT162b2, BioNTech i Pfizer havien dut a terme assajos de fase I sobre BNT162b1 a Alemanya i els Estats Units, mentre que Fosun va realitzar un assaig de fase I a la Xina. En aquests estudis de Fase I, BNT162b2 va demostrar tenir un millor perfil de seguretat que els altres tres candidats a BioNTech. [181][43][182][183]
L'assaig pivotal de fase II-III amb la candidata a vacuna principal "BNT162b2" va començar al juliol. Els resultats preliminars dels assaigs clĂnics de fase I-II sobre BNT162b2, publicats a l'octubre de 2020, van indicar potencial per a la seva seguretat i eficĂ cia. [43] Durant el mateix mes, l'AgĂšncia Europea del Medicament (EMA) va començar una revisiĂł periĂČdica de BNT162b2.[184]
L'estudi de BNT162b2 Ă©s un assaig en fase contĂnua en fase III a novembre de 2020. [44] Es tracta d'un "estudi aleatoritzat, controlat amb placebo, cec per a observadors, cerca de dosi, selecciĂł de candidats a vacuna i eficĂ cia en individus sans". [44] L'estudi es va ampliar a mitjans de 2020 per avaluar l'eficĂ cia i la seguretat de BNT162b2 en un major nombre de participants, arribant a desenes de milers de persones que van rebre vacunes de prova en diversos paĂŻsos en col·laboraciĂł amb Pfizer i Fosun. [46][130]
L'assaig de fase III avalua la seguretat, eficà cia, tolerabilitat i immunogenicitat de BNT162b2 a nivell mitjà (dues injeccions separades per 21 dies) en tres grups d'edat: 12-15 anys, 16-55 anys o més de 55 anys. [44] Els resultats de la fase III que indiquen una eficà cia del 95% de la vacuna desenvolupada es van publicar el 18 de novembre de 2020. [50] Per a la seva aprovació a la UE, l'EMA va confirmar una eficà cia global de la vacuna del 95%. [185] L'EMA va aclarir que la segona dosi s'hauria d'administrar tres setmanes després de la primera dosi. [186]
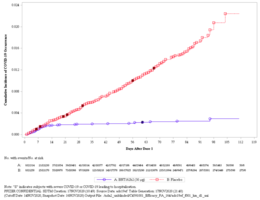 Corbes d'incidĂšncia acumulades per a infeccions simptomĂ tiques per COVID-19 desprĂ©s de la primera dosi de la vacuna de Pfizer-BioNTech (tozinameran) o placebo en un assaig clĂnic doble cec (vermell: placebo; blau: tozinameran)[187]
Corbes d'incidĂšncia acumulades per a infeccions simptomĂ tiques per COVID-19 desprĂ©s de la primera dosi de la vacuna de Pfizer-BioNTech (tozinameran) o placebo en un assaig clĂnic doble cec (vermell: placebo; blau: tozinameran)[187]
Als 14 dies després de la dosi 1, la incidÚncia acumulada comença a divergir entre el grup vacunat i el grup placebo. La major concentració d'anticossos neutralitzants s'aconsegueix 7 dies després de la dosi 2 en adults més joves i 14 dies després de la dosi 2 en adults majors. [185]
| Subgrup de punts finals | Eficà cia (interval de confiança del 95%) |
|---|---|
| Totes les edats | 95,0% (90,0â97,9%) |
| De 12 a 17 anys | No estimable[b] |
| 18â64 anys | 95,1% (89,6â98,1%) |
| 65â74 anys | 92,9% (53,1â99,8%) |
| Edat â„75 anys | 100,0% (â13,1 a 100,0%) |
| Totes les edats, desprĂ©s de la dosi 1, abans de la dosi 2 | 52,4% (29,5â68,4%) |
| Totes les edats, â„10 dies desprĂ©s de la dosi 1, abans de la dosi 2 | 86,7% (68,6â95,4%) |
| Totes les edats, <7 dies desprĂ©s de la dosi 2 | 90,5% (61,0â98,9%) |
| Totes les edats, â„7 dies desprĂ©s de la dosi 2 | 94,8% (89,8â97,6%) |
| Totes les edats, Estats Units | 94,9% (88,6â98,2%) |
| Totes les edats, Argentina | 97,2% (83,3â99,9%) |
| Totes les edats, Brasil | 87,7% (8,1â99,7%) |
L'assaig de fase III en curs, que està previst que s'executi del 2020 al 2022, està dissenyat per avaluar la capacitat de BNT162b2 per prevenir infeccions greus, aixà com la durada de l'efecte immunitari. [46][188][159]
L'activitat alta d'anticossos persisteix durant almenys tres mesos després de la segona dosi, amb una vida mitjana estimada dels anticossos de 55 dies. A partir d'aquestes dades, un estudi va suggerir que els anticossos podrien romandre detectables durant uns 554 dies. [189]
Pfizer i BioNTech van iniciar un assaig de control aleatoritzat de fase II-III en dones embarassades sanes de 18 anys o mĂ©s (NCT04754594). [190] L'estudi avaluarĂ 30 mcg de BNT162b2 o placebo administrats mitjançant injecciĂł intramuscular en dues dosis, amb 21 dies de diferĂšncia. La part de fase II de l'estudi inclourĂ aproximadament 350 dones embarassades aleatĂČries 1: 1 per rebre BNT162b2 o placebo a les 27 a 34 setmanes de gestaciĂł. La part de fase III d'aquest estudi avaluarĂ la seguretat, tolerabilitat i immunogenicitat de BNT162b2 o placebo entre les dones embarassades inscrites a les 24 a 34 setmanes de gestaciĂł. Pfizer i BioNTech van anunciar el 18 de febrer de 2021 que els primers participants van rebre la seva primera dosi en aquest assaig. [191]
Un estudi publicat el març del 2021 a l'American Journal of Obstetrics and Gynecology va arribar a la conclusiĂł que les vacunes d'ARN missatger contra el nou coronavirus, com les vacunes de Pfizer-BioNTech i Moderna, eren segures i efectives per proporcionar immunitat contra la infecciĂł a mares embarassades i lactants. A mĂ©s, van trobar que els anticossos naturals creats pel sistema immunitari de la mare es transmetien als seus fills a travĂ©s de la placenta i/o la llet materna, donant lloc aixĂ a una immunitat passiva entre el nen, donant efectivament protecciĂł al nen contra la malaltia. L'estudi tambĂ© va trobar que la immunitat induĂŻda per la vacuna entre els participants de l'estudi va ser mĂ©s forta d'una manera estadĂsticament significativa sobre la immunitat obtinguda a travĂ©s de la recuperaciĂł d'una infecciĂł natural per COVID-19. A mĂ©s, l'estudi va informar que l'apariciĂł i la intensitat dels possibles efectes secundaris en les persones sotmeses a embarĂ s o lactĂ ncia va ser molt similar a les esperades de les poblacions no embarassades, romanent en general molt lleus i ben tolerades, incloent principalment dolor al lloc de la injecciĂł, mals de cap menors, dolors musculars o fatiga durant un curt perĂode de temps. [192]
El gener del 2021, Pfizer va dir que havia acabat d'inscriure 2.259 nens d'entre 12 i 15 anys per estudiar la seguretat i l'eficà cia de la vacuna. [193] El 31 de març de 2021, Pfizer i BioNTech van anunciar a partir de les dades inicials de l'assaig de fase III que la vacuna és 100% efectiva per a persones de 12 a 15 anys, amb assajos per a aquells més joves encara en curs. [194]
Una carta d'investigaciĂł publicada a JAMA va informar que les vacunes semblaven ser segures per als receptors de trasplantaments d'ĂČrgans immunodeprimits, perĂČ que la resposta d'anticossos resultant va ser considerablement pitjor que en la poblaciĂł no immunodeprimida desprĂ©s d'una sola dosi. El document admetia la limitaciĂł de nomĂ©s revisar les dades desprĂ©s de la primera dosi d'una vacuna de cicle de dues dosis. [195]
El 2 de novembre de 2021, The BMJ va publicar un article del periodista Paul D. Thacker al·legant que hi ha hagut "males prà ctiques" a Ventavia, una de les empreses involucrades en els assajos d'avaluació de fase III de la vacuna de Pfizer. [196] L'informe va ser acollit amb entusiasme pels activistes antivacunes. David Gorski va comentar a Science-Based Medicine que l'article de Thacker presentava fets sense context necessari per a un efecte enganyós, jugant amb la gravetat dels problemes assenyalats. [197]
|
|||
Tot i que es desenvolupa conjuntament amb Pfizer,[198] Comirnaty es basa en la tecnologia d'ARNm propietĂ ria de BioNTech,[198] i BioNTech tĂ©Â l'autoritzaciĂł de comercialitzaciĂł als Estats Units, la UniĂł Europea, el Regne Unit i CanadĂ ; [198] llicĂšncies accelerades com l'autoritzaciĂł d'Ășs d'emergĂšncia dels EUA (EUA) es mantenen conjuntament amb Pfizer a molts paĂŻsos. [198]
L'AgĂšncia Reguladora de Medicaments i Productes Sanitaris del Regne Unit (MHRA) va donar a la vacuna "rĂ pida aprovaciĂł reguladora temporal per abordar problemes significatius de salut pĂșblica, com ara una pandĂšmia", el 2 de desembre de 2020, cosa que estĂ permesa en virtut de la Llei de medicaments de 1968. [57] Ăs la primera vacuna contra la COVID-19 aprovada per a Ășs nacional desprĂ©s de sotmetre's a assajos a gran escala,[199] i la primera vacuna d'ARNm autoritzada per al seu Ășs en humans. [57][200] El Regne Unit es va convertir aixĂ en el primer paĂs occidental a aprovar una vacuna contra la COVID-19 per a Ășs nacional,[201] tot i que la decisiĂł d'accelerar la vacuna va ser criticada per alguns experts. [202]
DesprĂ©s del Regne Unit, els segĂŒents paĂŻsos i regions van accelerar els processos per aprovar la vacuna PfizerâBioNTech COVID-19 per al seu Ășs: Argentina,[203] AustrĂ lia,[204] Bahrain,[205] CanadĂ ,[206][207] Xile,[208] Costa Rica,[209] Equador,[208] Hong Kong,[210] Iraq,[211] Israel,[212] JordĂ nia,[213] Kuwait,[214] MalĂ isia,[215] MĂšxic,[216][217] Oman,[218] PanamĂ ,[219] Filipines,[220] Qatar,[221] ArĂ bia Saudita,[222][223][224] Singapur,[225][226][227] Corea del Sud,[228][229] els Emirats Ărabs Units,[230] els Estats Units,[231] i Vietnam. [232]
L'OrganitzaciĂł Mundial de la Salut (OMS) el va autoritzar per a Ășs d'emergĂšncia. [233][234][235][236]
Als Estats Units, una autoritzaciĂł d'Ășs d'emergĂšncia (EUA) Ă©s "un mecanisme per facilitar la disponibilitat i l'Ășs de contramesures mĂšdiques, incloses les vacunes, durant emergĂšncies de salut pĂșblica, com l'actual pandĂšmia de COVID-19", segons l'AdministraciĂł d'Aliments i Medicaments (FDA). [237] Pfizer va sol·licitar un EUA el 20 de novembre de 2020,[238] i la FDA va aprovar la sol·licitud tres setmanes desprĂ©s, l'11 de desembre de 2020. El ComitĂš Assessor sobre PrĂ ctiques d'ImmunitzaciĂł (ACIP) dels Centres per al Control i la PrevenciĂł de Malalties (CDC) dels Estats Units va aprovar recomanacions per a la vacunaciĂł de les persones de setze anys o mĂ©s. [239][240] DesprĂ©s de l'emissiĂł als EUA, BioNTech i Pfizer van continuar l'assaig clĂnic de fase III per finalitzar les dades de seguretat i eficĂ cia, cosa que va conduir a la sol·licitud de llicĂšncia (aprovaciĂł) de la vacuna als Estats Units. [237][30][146] El 10 de maig de 2021, la FDA nord-americana tambĂ© va autoritzar la vacuna per a persones de 12 a 15 anys sota un EUA ampliat. [241][30][146][242][147] La recomanaciĂł de la FDA va ser aprovada per l'ACIP i adoptada pels CDC el 12 de maig de 2021. [243][244] A l'octubre de 2021, l'EUA es va ampliar per incloure nens de 5 a 11 anys d'edat. [245] El juny de 2022, l'EUA es va ampliar per incloure nens de sis mesos a quatre anys d'edat. [28]
El 16 de febrer de 2021, l'Autoritat Reguladora de Productes Sanitaris de Sud-Ă frica (SAHPRA) de Sud-Ă frica va emetre la secciĂł 21, AprovaciĂł d'Ășs d'emergĂšncia per a la vacuna. [246][247]
El 5 de maig de 2021, Health Canada va autoritzar la vacuna per a persones de 12 a 15 anys. [248][249] El 18 de maig de 2021, l'Autoritat de CiÚncies de la Salut de Singapur va autoritzar la vacuna per a persones de 12 a 15 anys. [250] L'AgÚncia Europea del Medicament (EMA) va fer el mateix el 28 de maig de 2021. [251]
El 4 de juny de 2021, l'AgĂšncia Reguladora de Medicaments i Productes Sanitaris del Regne Unit (MHRA) va prendre una decisiĂł similar i va aprovar l'Ășs de la vacuna per a persones de dotze anys o mĂ©s. [23][104][105]
El 19 de desembre de 2020, l'AgĂšncia SuĂŻssa de Productes TerapĂšutics (Swissmedic) va concedir l'autoritzaciĂł temporal per a la vacuna Pfizer-BioNTech COVID-19 per a Ășs regular, dos mesos desprĂ©s de rebre la sol·licitud, dient que la vacuna complia plenament els requisits de seguretat, eficĂ cia i qualitat. [38][252][253][254][255][256][257] Aquesta Ă©s la primera autoritzaciĂł sota un procediment estĂ ndard. [38][252]
El 21 de desembre de 2020, el ComitĂš de Medicaments d'Ăs HumĂ (CHMP) de l'AgĂšncia Europea del Medicament (EMA) va recomanar concedir l'autoritzaciĂł condicional de comercialitzaciĂł de la vacuna Pfizer-BioNTech COVID-19 sota la marca Comirnaty. [2][258][3] La recomanaciĂł va ser acceptada per la ComissiĂł Europea el mateix dia. [258][259]
El 23 de febrer de 2021, l'AgĂšncia Brasilera de RegulaciĂł SanitĂ ria va aprovar la vacuna Pfizer-BioNTech COVID-19 sota el seu procediment estĂ ndard d'autoritzaciĂł de comercialitzaciĂł. [260][261][262][263] El juny de 2021, l'aprovaciĂł es va ampliar als majors de dotze anys. [264][265] El procĂ©s de negociaciĂł de Pfizer amb Brasil (i altres paĂŻsos llatinoamericans) va ser descrit com a "assetjament escolar". El contracte prohibeix a l'estat del Brasil discutir pĂșblicament l'existĂšncia o els termes del seu acord amb Pfizer-BioNTech sense el consentiment per escrit del primer. Brasil tambĂ© va tenir restringit donar o rebre donacions de vacunes. [266][267]
El juliol de 2021, l'AdministraciĂł d'Aliments i Medicaments dels Estats Units (FDA) va concedir una designaciĂł de revisiĂł prioritĂ ria per a la sol·licitud de llicĂšncia biolĂČgica (BLA) per a la vacuna Pfizer-BioNTech COVID-19 amb una data objectiu per a la decisiĂł el gener de 2022. [268][269] El 23 d'agost de 2021, la FDA va aprovar la vacuna per al seu Ășs per a majors de setze anys. [29][63][26]
La vacuna contra la COVID-19 de Pfizer-BioNTech Comirnaty es va autoritzar al Canadà el setembre del 2021 per a persones de dotze anys o més. [18][19][17][270]
El juliol del 2022, la FDA va aprovar la vacuna per al seu Ășs per a majors de dotze anys. [271][26]
El setembre del 2022, el CHMP de l'EMA va recomanar convertir les autoritzacions condicionals de comercialització de la vacuna en autoritzacions està ndard de comercialització. [37] La recomanació cobreix totes les vacunes adaptades existents i properes de Comirnaty, incloses les adaptades Comirnaty Original/Omicron BA.1 (tozinameran/riltozinameran) i Comirnaty Original/Omicron BA.4/5 (tozinameran/famtozinameran). [2][37]
El juliol del 2021, el primer ministre d'Israel va anunciar que el paĂs estava desplegant una tercera dosi de la vacuna de Pfizer-BioNTech a les persones majors de 60 anys, basant-se en dades que suggerien una important disminuciĂł de la immunitat contra la infecciĂł amb el temps per a aquells amb dues dosis. [272] El paĂs va ampliar la disponibilitat a tots els israelians majors de 12 anys, desprĂ©s de cinc mesos des del seu segon tret. El 29 d'agost de 2021, el tsar del coronavirus d'Israel va anunciar que els israelians que no haguessin rebut una dosi de reforç en els sis mesos posteriors a la segona dosi perdrien l'accĂ©s al passaport de vacunes del passi verd del paĂs. [273] Els estudis realitzats a Israel van trobar que una tercera dosi reduĂŻa la incidĂšncia de malalties greus. [274]
L'agost de 2021, el Departament de Salut i Serveis Humans dels Estats Units (HHS) va anunciar un pla per oferir una dosi de reforç vuit mesos desprĂ©s de la segona dosi, citant proves de protecciĂł reduĂŻda contra la malaltia lleu i moderada i la possibilitat d'una protecciĂł reduĂŻda contra la malaltia greu, l'hospitalitzaciĂł i la mort. [275] L'AdministraciĂł d'Aliments i Medicaments dels Estats Units (FDA) i els Centres per al Control i la PrevenciĂł de Malalties (CDC) van autoritzar l'Ășs d'una dosi addicional de vacuna d'ARNm per a persones immunodeprimides en aquell moment. [75][76] Els cientĂfics i l'OMS van assenyalar l'agost de 2021 la manca d'evidĂšncia sobre la necessitat d'una dosi de reforç per a persones sanes i que la vacuna continua sent eficaç contra la malaltia greu mesos desprĂ©s de l'administraciĂł. [276] En un comunicat, l'OMS i el Grup Assessor EstratĂšgic d'Experts (SAGE) van dir que, tot i que la protecciĂł contra la infecciĂł pot disminuir, Ă©s probable que es mantingui la protecciĂł contra la malaltia greu a causa de la immunitat mediada per cĂšl·lules. [277] La investigaciĂł sobre el moment ĂČptim per als impulsors estĂ en curs, i un reforç massa aviat pot conduir a una protecciĂł menys robusta. [278]
El setembre del 2021, les autoritzacions de la FDA i els CDC es van ampliar per proporcionar una tercera dosi per a altres grups especĂfics. [279][280][281]
L'octubre del 2021, l'AgÚncia Europea del Medicament (EMA) va declarar que es podia administrar una dosi de reforç de la vacuna a persones sanes, de 18 anys o més, almenys sis mesos després de la segona dosi. [77] També va afirmar que les persones amb sistemes immunitaris "greument debilitats" poden rebre una dosi addicional de la vacuna de Pfizer-BioNTech o de la vacuna de Moderna a partir d'almenys 28 dies després de la seva segona dosi. [77] L'aprovació final per proporcionar trets de reforç a la Unió Europea serà decidida per cada govern nacional. [282]
L'octubre del 2021, la FDA i el CDC van autoritzar l'Ășs de dosis de reforç de la vacuna homĂČlogues o heterĂČlogues. [283][284][285]
L'octubre del 2021, l'Administració de Productes TerapÚutics d'Austrà lia (TGA) va aprovar provisionalment una dosi de reforç de Comirnaty per a persones de 18 anys o més. [286][287]
El gener del 2022, la FDA va ampliar l'autoritzaciĂł d'Ășs d'emergĂšncia per preveure l'Ășs d'una dosi de reforç de la vacuna als joves de 12 a 15 anys i va escurçar el perĂode d'espera desprĂ©s de la primovacunaciĂł a cinc mesos a partir dels sis mesos. [288][289][290][291]
El maig del 2022, la FDA va ampliar l'autoritzaciĂł d'Ășs d'emergĂšncia per preveure l'Ășs d'una dosi de reforç de la vacuna a les persones de 5 a 11 anys. [292]
L'agost del 2022, la FDA va revocar l'autoritzaciĂł d'Ășs d'emergĂšncia del reforç de la vacuna monovalent per a persones de dotze anys o mĂ©s i la va substituir per una autoritzaciĂł d'Ășs d'emergĂšncia per a la dosi de reforç de la vacuna bivalent per al mateix grup d'edat. [65]
L'octubre del 2021, l'AdministraciĂł d'Aliments i Medicaments dels Estats Units (FDA) i els Centres per al Control i la PrevenciĂł de Malalties (CDC) van autoritzar l'Ășs de dosis de reforç de vacunes homĂČlogues o heterĂČlogues. [283][284] L'autoritzaciĂł es va ampliar a tots els adults el novembre de 2021. [285]
L'agost de 2022, la "Vacuna Pfizer-BioNTech COVID-19, bivalent (original i ĂČmicron BA.4/BA.5)" (en resum: "Vacuna COVID-19, Bivalent") va rebre una autoritzaciĂł d'Ășs d'emergĂšncia de l'AdministraciĂł d'Aliments i Medicaments dels Estats Units (FDA) per utilitzar-la com a dosi de reforç en persones de dotze anys o mĂ©s. Una dosi contĂ© 15 mcg d'"un ARN missatger modificat per nucleĂČsids (modRNA) que codifica la glicoproteĂŻna espiga viral (S) de la soca Wuhan-Hu-1 del SARS-CoV-2 (original)" i 15 mcg "de modRNA que codifiquen la glicoproteĂŻna S dels llinatges BA.4 i BA.5 de la variant ĂČmicron del SARS-CoV-2 BA.4 i BA.5". [293]
La vacuna bivalent autoritzada als Estats Units Ă©s diferent de la que es va autoritzar per al seu Ășs al Regne Unit,[70] ja que aquesta Ășltima contĂ© com a segon component de modRNA 15 mcg de modRNA que enocodifiquen la gylcoproteĂŻna S de l'anterior variant BA.1. [70]
El setembre del 2022, la Unió Europea va autoritzar tant la BA.1 com les versions de reforç BA.4/BA.5 de la vacuna bivalent per a persones de dotze anys o més. [2][3][72]
Tot i que la vacuna BA.1 d'ĂČmicron s'ha provat en un estudi clĂnic, la vacuna BA.4/BA.5 d'ĂČmicron nomĂ©s es va provar en estudis preclĂnics. Segons la presentaciĂł publicada,[294] s'han explorat en un estudi amb ratolins BALB/c-ratolins les respostes de neutralitzaciĂł d'ĂČmicron BA.4/BA.5 monovalent, ĂČmicron BA.4/BA.5 bivalent i la vacuna original BNT162b2. [295][296]
L'octubre del 2022, la FDA va modificar l'autorització del reforç bivalent per cobrir les persones de cinc anys o més. [297]
El desembre del 2022, la FDA va modificar l'autorització perquÚ el reforç bivalent s'utilitzés com a tercera dosi en persones de sis mesos a quatre anys. [298]
El setembre del 2023, l'FDA va aprovar una versiĂł actualitzada de la variant monovalent (Ășnica) d'ĂČmicron XBB.1.5 de la vacuna (fĂłrmula Comirnaty 2023-2024) com a dosi Ășnica per a persones de dotze anys o mĂ©s; [26] i va autoritzar la fĂłrmula Pfizer-BioNTech COVID-19 Vaccine 2023â2024 sota Ășs d'emergĂšncia per a persones de 6 mesos a 11 anys d'edat. [25][299] Es van revocar les aprovacions i autoritzacions d'emergĂšncia per a les versions bivalents de la vacuna. [25] Health Canada va aprovar la subvariant Pfizer-BioNTech Comirnaty Omicron XBB.1.5, vacuna monovalent contra la COVID-19 el setembre de 2023. [18] L'AgĂšncia Reguladora de Medicaments i Productes Sanitaris del Regne Unit va aprovar l'Ășs de la vacuna Comirnaty Omicron XBB.1.5 el setembre de 2023. [300][301]
Prop de 649 milions de dosis de la vacuna contra la COVID-19 de Pfizer-BioNTech, inclosos uns 55 milions de dosis en nens i adolescents (menors de 18 anys) es van administrar a la UE/EEE des de l'autorització fins al 26 de juny de 2022. [302]
 Comirnaty
Comirnaty
BNT162b2 va ser el nom en clau durant el desenvolupament i les proves,[43][53] tozinameran és el nom internacional no propietari (INN),[36][303] i Comirnaty és el nom de la marca. [38][2] Segons BioNTech, el nom Comirnaty "representa una combinació dels termes COVID-19, ARNm, comunitat i immunitat". [304][305]
Famtozinameran Ă©s l'INN per a la variant BA.5 en la versiĂł bivalent de la vacuna. [306][307][308][309][6]
Raxtozinameran Ă©s l'INN per a la versiĂł de la variant XBB 1.5 de la vacuna. [36][310][311][312][6]
Pfizer va reportar ingressos de 154 milions de dĂČlars de la vacuna contra la COVID-19 de Pfizer-BioNTech el 2020,[176] i 36.000 milions de dĂČlars el 2021. [313][314]
El juliol del 2020, el programa de desenvolupament de vacunes Operation Warp Speed va fer una comanda anticipada de 1.950 milions de dĂČlars amb Pfizer per fabricar 100 milions de dosis d'una vacuna contra la COVID-19 per al seu Ășs als Estats Units si es demostrava que la vacuna era segura i eficaç. [42][315][316][317][318] A mitjans de desembre de 2020, Pfizer tenia acords per subministrar 300 milions de dosis a la UniĂł Europea,[319] 120 milions de dosis al JapĂł,[320] 40 milions de dosis (10 milions abans del 2021) al Regne Unit,[159] 20 milions de dosis al CanadĂ ,[321] un nombre no especificat de dosis a Singapur,[322] i 34,4 milions de dosis a MĂšxic. [323] Fosun tambĂ© tĂ© acords per subministrar 10 milions de dosis a Hong Kong i Macau. [324]
Els relats sobre com Pfizer es va obrir camĂ en un gran acord per proporcionar 1.800 milions de dosis de la seva vacuna a la UniĂł Europea van ser descrits pel New York Times com "una sorprenent alineaciĂł de supervivĂšncia polĂtica i enrenou corporatiu". [325]
Pfizer ha estat acusada d'obstaculitzar l'equitat de les vacunes. El 2021, Pfizer va lliurar només el 39% de les dosis acordades contractualment al programa COVAX, una xifra que equival a l'1,5% de totes les vacunes produïdes per Pfizer. La companyia va vendre el 67% de les seves dosis a països d'alts ingressos i no en va vendre cap directament a països de baixos ingressos. [326]
Pfizer va pressionar activament contra l'aixecament temporal dels drets de propietat intel·lectual que permetria que la vacuna fos produïda per altres persones sense haver de pagar una quota de drets d'autor. [327][328]
Al voltant del maig del 2021 van circular vĂdeos en plataformes per compartir vĂdeos que mostraven persones amb imants enganxats als braços desprĂ©s de rebre la vacuna, cosa que suposadament demostrava la teoria de la conspiraciĂł que les vacunes contenen microxips, perĂČ aquests vĂdeos han estat desmentits. [329][330][331][332]
Afegeix-hi un comentari: